[Música] te has preguntado cómo están hechos los objetos que ves todos los días esta pregunta se la hacían desde hace muchos años uno de los primeros filósofos en hacerse esa pregunta fue demócrito que decía que al dividir la materia llegaríamos a una última particular sólida e indestructible a esta particular la llamo átomo que significa indivisible sin embargo esta definición sólo sería una pequeña parte de los descubrimientos que se hicieron tiempo después en 1808 el científico inglés john dalton definió de una forma más precisa las unidades indivisibles con las que está hecha la materia su modelo
atómico definía lo siguiente los elementos están formados por partículas diminutas indivisibles e indestructibles llamadas átomos todos los átomos del mismo elemento son idénticos tienen igual tamaño masa y propiedades químicas por lo tanto los átomos de distintos elementos presentan propiedades diferentes y los compuestos químicos se forman al unirse dos o más átomos de diferentes elementos en proporciones fijas [Música] donde la relación de átomos será un número entero o una pasión sencilla una reacción química implica sólo la separación combinación o reordenamiento de los átomos nunca supone la creación o destrucción de los mismos [Música] a pesar de
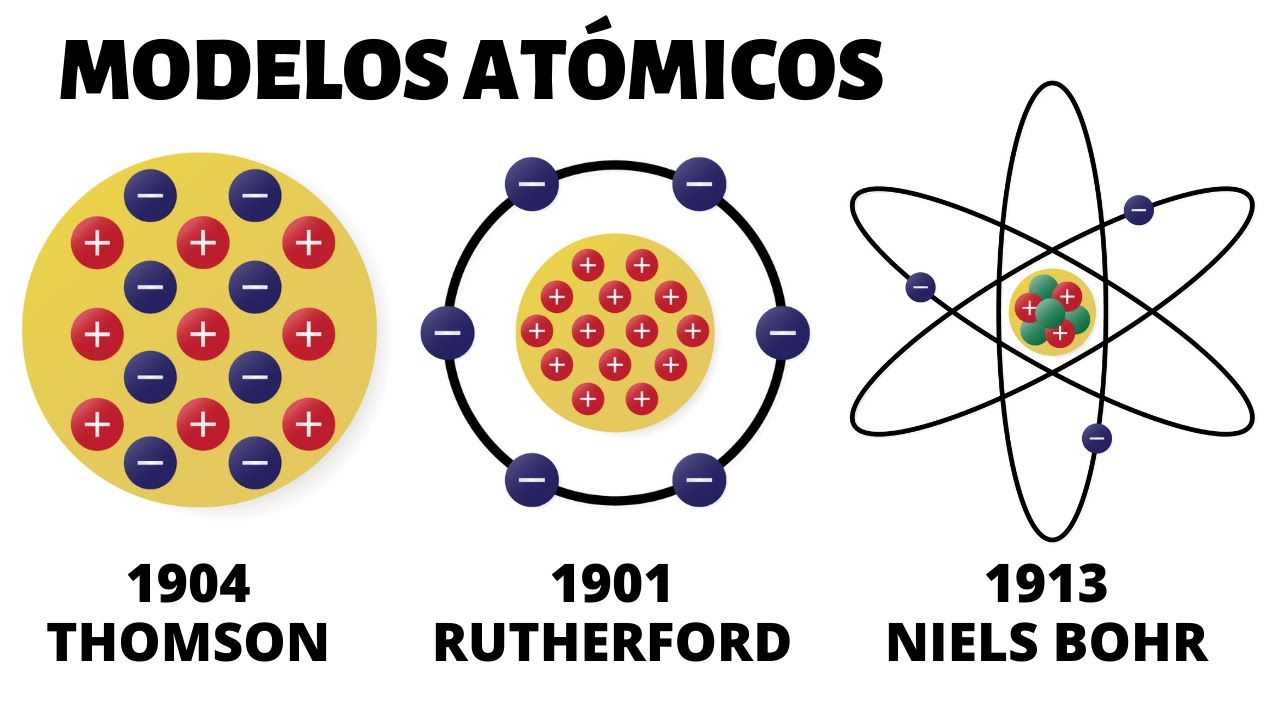
las teorías de demócrito y dalton sobre el átomo como partícula indivisible una serie de investigaciones demostraron que el átomo contaba con partículas más pequeñas en 1890 el científico joseph thompson mientras estudiaba en la radiación a través del magnetismo se dio cuenta que había una repulsión de los rayos catódicos como un imán en donde supuso que debían de haber partículas negativas y fluía en esa habitación su modelo atómico proponía lo siguiente el átomo es una esfera de electricidad positiva en donde se encuentran los electrones [Música] a las partículas eléctricamente negativas las llamo electrones [Música] aún reconocía
al átomo como una partícula compacta e indivisible thomson propuso un modelo atómico semejante a una gelatina con pasas por lo que en 1906 cuando el premio nobel de física por descubrir el electrónico después del descubrimiento del electrón el científico neozelandés ernest rutherford se propuso a estudiar la estructura interna del átomo schubert fort hizo pasar partículas alfa sobre una lámina de oro observando que algunas partículas se desviaban con un ángulo muy grande descubriendo que el átomo tenía espacios vacíos y proponiendo que las cargas positivas se encontraban concentradas en un pequeño núcleo su modelo atómico consistía en
que el átomo estaba formado de un pequeño núcleo con carga positiva y alrededor de él se encontraban los electrones dispersos con diferentes trayectorias [Música] también proponía que casi toda la masa se encontraba en el núcleo a las cargas positivas las llamo protones para este entonces investigaciones anteriores suponían que si los átomos eran neutros debían de tener el mismo número de cargas positivas que los electrones para poder tener estabilidad el descubrimiento de rutherford le valió el premio nobel de física en 1908 por sus investigaciones sobre la estructura del núcleo atómico sabiendo que la carga positiva se
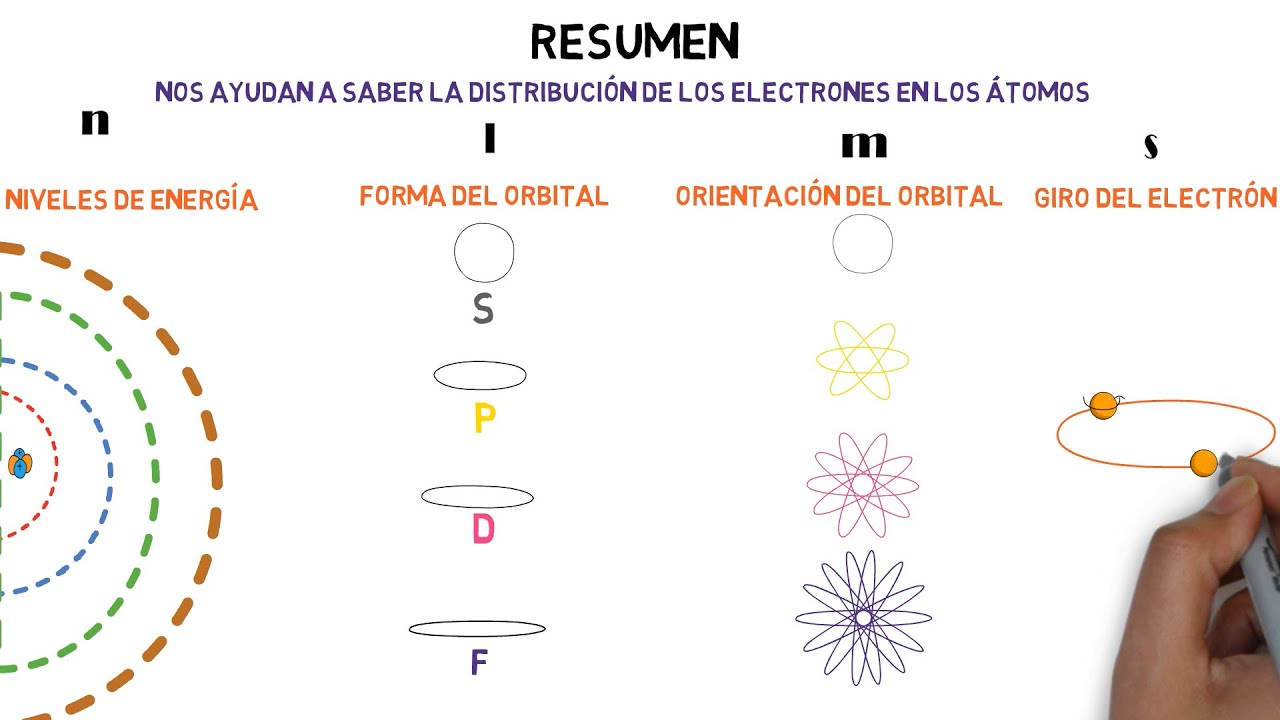
encontraba en el núcleo y la negativa estaba alrededor de él los científicos no podían comprender por qué el electrón no llegaba hasta el núcleo donde está el protón y colisionaba con él en 1913 el físico de al mes main sport desarrolló un modelo atómico abordando un modelo planetario donde el núcleo es el sol y los electrones de los planetas que giran alrededor él propuso que el electrón solo puede ocupar ciertas órbitas de energía específicas 1 electrón puede alcanzar niveles de energía más altos cuando ésta absorbe radiación este exceso de energía excita al átomo para que
pueda pasar de una órbita a otra por el contrario cuando el electrón regresa a su órbita original este emite la energía absorbida en forma de fotón también asignó un número a cada nivel de energía el cual solo podía tener un número determinado de electrones [Música] en 1922 recibió el premio nobel de física por su aportación al comportamiento del átomo y la mecánica cuántica a pesar de la aceptación de los modelos anteriores éstos generaban un grande problema sin resolver y este era el peso de los átomos [Música] en 1932 el físico inglés james chadwick bombardeo una
lámina delgada de berilio con partículas sal para el metal emite una radiación muy alta similar a los rayos gamma los siguientes experimentos demostraron que esos rayos en realidad eran tercer tipo de partículas subatómicas sin carga eléctrica por lo que en 1932 propuso su modelo atómico el cual determinó que los neutrones son partículas subatómicas que no tienen carga eléctrica y cuya masa es ligeramente mayor a la de los protones que casi toda la masa se concentraba en el núcleo a estas partículas hallamos neutrones ya que son partículas neutras este descubrimiento le valió el premio nobel de
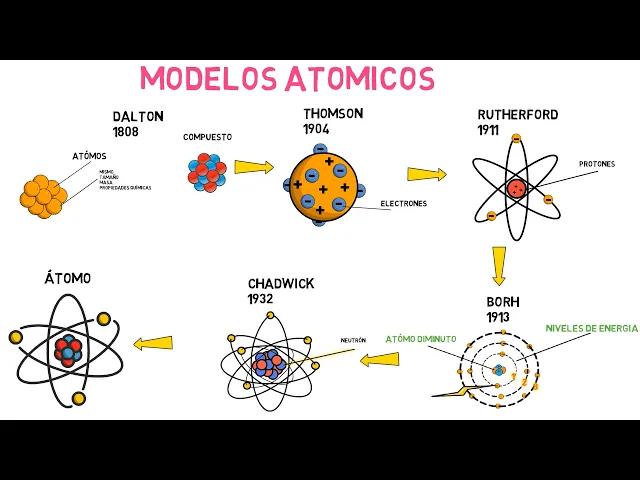
física en 1935 por descubrir el neutrón con este modelo se resolvía el misterio del por qué el helio con dos protones pesaba cuatro veces más que el hidrógeno con un protón suponiendo que la masa de los electrones es despreciable ahora se sabía que el neutrón con masa similar le daba ese peso extra ya que el libro que no obtiene neutrón [Música] estos modelos atómicos e investigaciones aleatorias ayudaron a un mejor entendimiento de cómo está hecha la materia dalton con su definición de átomo thompson con el descubrimiento del electrón rutherford con el descubrimiento del protón worth
con su modelo planetario y niveles energéticos y chadwick con el descubrimiento del neutrón sentaron las bases de lo que conocemos hoy como átomo [Música] si te gustó este vídeo dale like y suscríbete no olvides dejar tu comentario nos vemos hasta el próximo vídeo [Música]





![🌐Modelos Atómicos🌐 [Fácil y Rápido] | QUÍMICA | FÍSICA |](https://img.youtube.com/vi/LS3N5hOxRPE/maxresdefault.jpg)




![Chemistry course from 0 ✅ [COMPLETED AND RE-EDITED]](https://img.youtube.com/vi/2jyxYUQXKBQ/maxresdefault.jpg)