Una de las aportaciones al estudio de la naturaleza del enlace químico la hizo el bioquímico estadounidense Linus Carl Pauling quien estudió los trabajos de Lewis y propuso el concepto de electronegatividad en 1932. La electronegatividad es la capacidad que tiene un átomo para atraer electrones hacia así mismo. Pauling calculó las electronegatividades de los elementos químicos que iba desde 0.
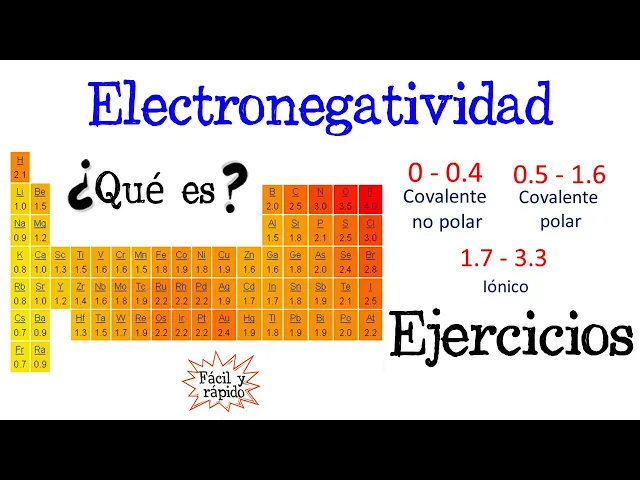
7 para los elementos menos electronegativos los cuales son Cesio y Francio, hasta 4 para el más electronegativo que es el Flúor. En la tabla periódica mientras hacia la derecha y hacia arriba esté un elemento químico mayor será su electronegatividad o sea mayor será su fuerza para atraer a los electrones de otros elementos químicos. Los gases nobles al tener lleno su último nivel de energía no se enlazan con otros elementos, es por esta razón que no aparecen en esta tabla.
Esta tabla te la estaré dejando en la caja de información para que puedas descargarla. Para determinar la naturaleza y el tipo de enlace químico con el que están unidos dos elementos se deben restar las electronegatividades de los elementos químicos participantes y si la diferencia de electronegatividad es de 0 a 0. 4 quiere decir que el enlace químico es de tipo covalente no polar, esto quiere decir que la fuerza de ambos elementos es similar y los electrones giran de igual manera en ambos elementos.
Si la diferencia de electronegatividad es entre 0. 5 y 1. 6 quiere decir que el enlace químico es de tipo covalente polar, esto quiere decir que un elemento químico es más fuerte que el otro y los electrones están más cerca del elemento más fuerte provocando que en ese extremo se produzca una ligera carga negativa por la cercanía de los electrones y del otro extremo se produzca una ligera carga positiva al estar más retirado sus electrones, es decir se forman dos polos uno positivo y otro negativo, es por eso que se llama enlace covalente polar porque hay dos polos, este símbolo es una letra griega llamada delta y significa carga parcial.
Si la diferencia de electronegatividad es entre 1. 7 y 3. 3 quiere decir que el enlace químico es de tipo iónico, esto quiere decir que un elemento es mucho más fuerte que el otro y termina quitándole el electrón al otro elemento formando un ion positivo y otro negativo.
Ahora te lo explico mediante unos ejemplos: Tenemos el flúor molecular, este dos quiere decir que el flúor está unido a otro flúor, nos fijamos en la tabla de electronegatividades que el flúor tiene una electronegatividad de 4, hacemos la resta 4 – 4 y el resultado es 0 y como podemos observar el enlace químico formado es de tipo covalente no polar. En el óxido de aluminio la electronegatividad del aluminio es 1. 5 y la del oxígeno es 3.
5, no importa el número de átomos que tenga el compuesto siempre el número de electronegatividad será el mismo, en estos ejercicios siempre al número mayor se la va restar el número menor, o sea a 3. 5 le restaremos 1. 5 y el resultado es 2, entonces el enlace es de tipo iónico.
En el pentacloruro de arsénico la electronegatividad del arsénico es 2 y la del cloro es 3, hacemos la resta y el resultado es 1, entonces el enlace es de tipo covalente polar. Para la molécula del agua El hidrógeno tiene una electronegatividad de 2. 1 y el oxígeno de 3.
5, hacemos la resta y el resultado es 1. 4, entonces el enlace es de tipo covalente polar. En el metano el carbono tiene una electronegatividad de 2.
5 y el hidrógeno de 2. 1, hacemos la resta y el resultado es de 0. 4, entonces el enlace es de tipo covalente no polar.
Y por último el cloruro de sodio, el sodio tiene una electronegatividad de 0. 9 y el cloro de 3, hacemos la resta y el resultado es 2. 1, entonces el enlace es de tipo iónico.

![🌿¿Qué es un Ecosistema Artificial?⚙️ EJEMPLOS [Fácil y Rápido] | BIOLOGÍA |](https://img.youtube.com/vi/OuDSVBh205Q/mqdefault.jpg)