o Olá pessoal nossa aula prática de hoje será sobre Protein veremos na prática é como se dá o processo de desnaturação de uma proteína contaremos com a ajuda da aluna Jéssica Costa do 6º semestre de enfermagem e para experimento de hoje utilizaremos a clara do ovo primeiro passo colocaremos uma solução fisiológica cloreto de sódio 0,9 por cento misturarem e E aí E aí E aí e agora pegaremos 2 ml dessa solução e colocaremos no tubo de ensaio e nós queremos aquecer na vontade e E aí [Música] E aí e agora iríamos Pegar 2 ml dessa
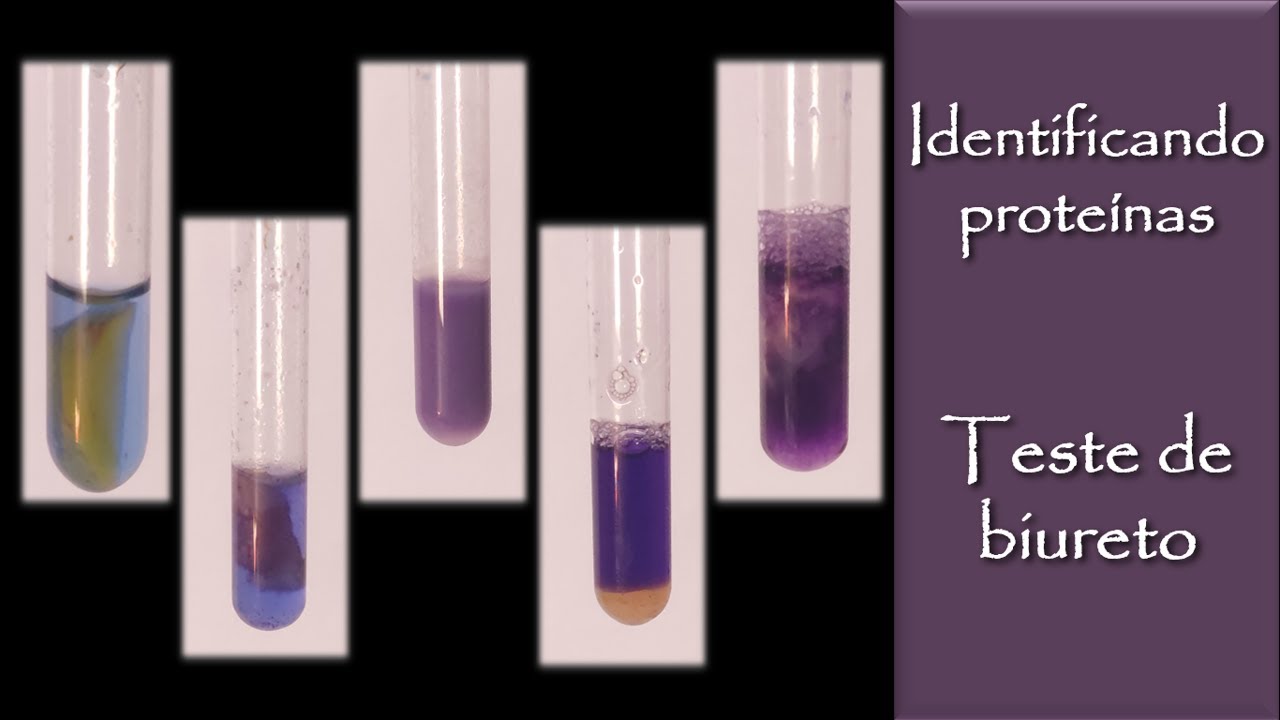
mesma solução e colocaremos 2 ml tem cada um dos vidros de relógio e E aí é o primeiro vídeo de relógio colocaremos etanol e e o segundo vida de relógio colocar Mc ácido tricloroacético e e no terceiro vidro de relógio colocaremos acetato de chumbo o E aí e perceba o que a clara de ovo Inclusive a que foi aquecida em contato com as soluções adquiriram por esbranquiçados para entendermos o que aconteceu vamos relembrar que as proteínas possuem estrutura primária secundária e terciária algumas proteínas ainda apresentam estrutura quaternária a estrutura primária nada mais é do que
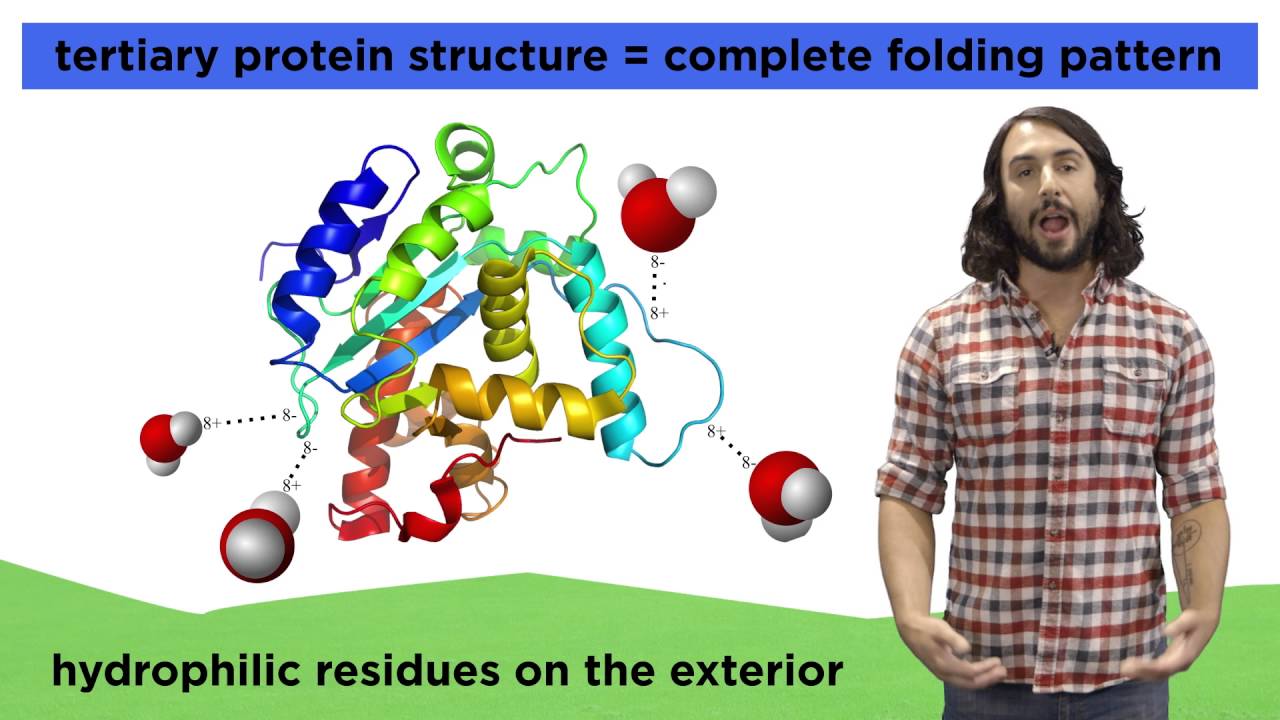
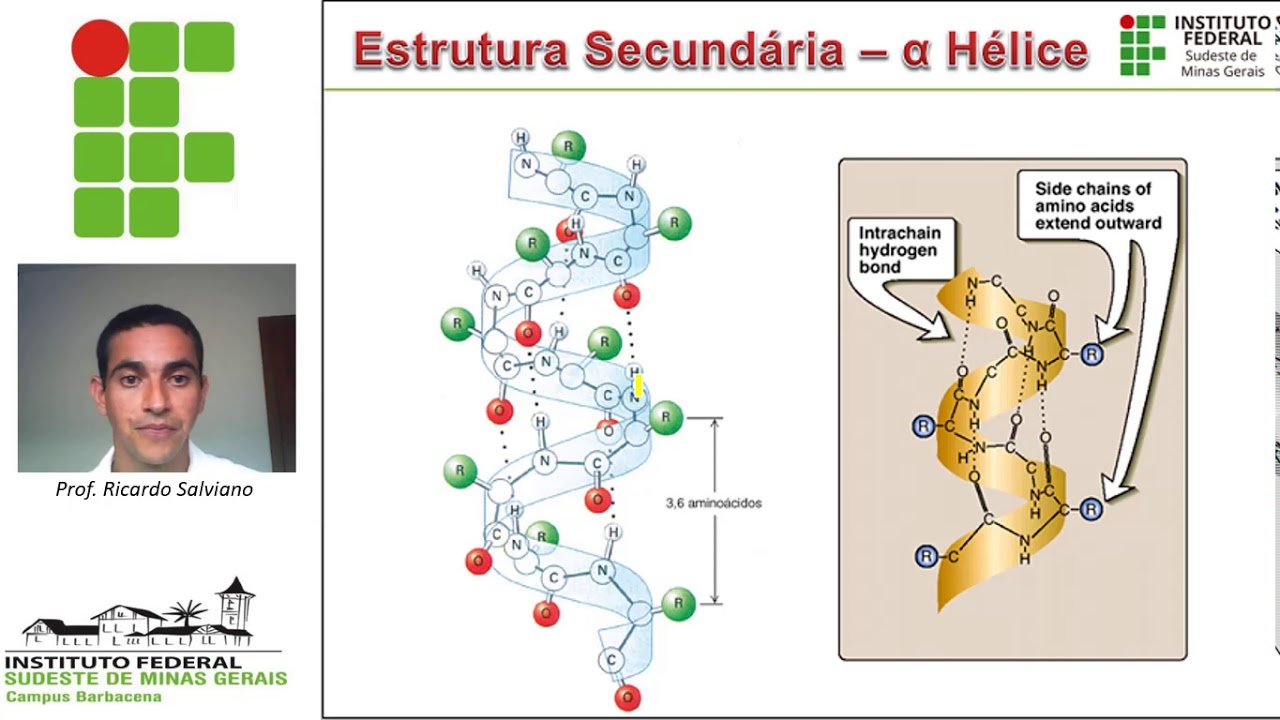
a sequência de aminoácidos que constitui a sua cadeia a estrutura secundária é a forma que essa cadeia assumir no espaço nesse exemplo do slide temos uma estrutura secundária em Eles já a estrutura terciária é a sua conformação é a forma que essa cadeia assumir no espaço em virtude da interação entre os seus grupamentos é esses laje nos mostra alguns tipos de interações que ocorrem entre aminoácidos de uma a cadeia proteica aqui em amarelo nós temos as ligações de hidrogênio ou Pontes de hidrogênio em azul as ligações de dissulfeto aqui em cima em laranja nós temos
um grupamento R carregado positivamente o grupamento R carregado negativamente de um outro aminoácido e ele se atraem e em verde nós temos representado uma interação hidrofóbica entre dois grupamentos R hidrofóbicos São essas interações que determinam a atração ou repulsão entre os grupamentos é e que vão determinar Qual é a forma que essa proteína assumirá no espaço qualquer ruptura dessas interações vai levar a uma quebra desta conformação levando à perda da função da proteína esse processo é chamado de desnaturação a desnaturação nada o que a perda da estrutura tridimensional da proteína capaz de levar a uma
perda da sua função as estruturas primárias e secundárias não são afetadas apenas a sua conformação e essa perda na sua conformação leva à perda da sua função biológica na maioria das vezes a desnaturação é um processo Irreversível existem vários agentes o condições desnaturantes para uma proteína na aula de hoje nós utilizamos alguns desses fatores ou agentes desnaturantes quando aquecemos a clara de ovo no tubo de ensaio o calor foi o fator desnaturante quando e levamos a temperatura aumentamos a vibração molecular e aí interações mais fracas como Pontes de hidrogênio ligações de hidrogênio se rompem alterando
a conformação da proteína quando co a salvo sobre a clara do ovo fizemos uso de um solvente orgânico os solventes orgânicos são desnaturadas Por que promovem a ruptura das pontes de hidrogênio ou das ligações de hidrogênio formando ligações em seu lugar veja na figura uma proteína na sua forma Nativa do lado esquerdo e na presença de um álcool essa ponte de hidrogênio sofreu uma ruptura e o álcool fez a ligação em seu lugar tanto de um lado quanto do outro esta ruptura Altera a conformação da proteína Este é um dos mecanismos pelo qual óculos 70
é capaz de eliminar o coronavírus ele promove uma ruptura das pontes de hidrogênio das proteínas externas do coronelismo mas no caso do coronavírus um outro mecanismo de ação sabemos que este vírus tem uma camada Ester Olá eu sou dentes orgânicos conseguem dissolver essa camada lipídica já o ácido tricloroacético promoveu desnaturação pela alteração do PH ácidos ou bases fortes alteram o estado de ionização dos grupamentos R E assim eles vão alterar a atração ou a repulsão que determinava aquela conformação da proteína já quando pingamos acetato de chumbo o agente desnaturante foi o chumbo o metal pesado
os metais pesados em solução possuem carga e são atraídos pelos grupamentos RD carga negativo a figura nos dá o exemplo do mercúrio no nosso caso utilizamos o chumbo mas o processo é o mesmo ele forma um complexo com os grupamentos R que precipita essa proteína por hoje é isso Pessoal espero que tenham gostado até a próxima aula se inscreva no canal deixe o seu like compartilhe com os colegas e fiquem ligados para os próximos vídeos aqui de bioquímica usem mas quando forem sair de casa e [Música]