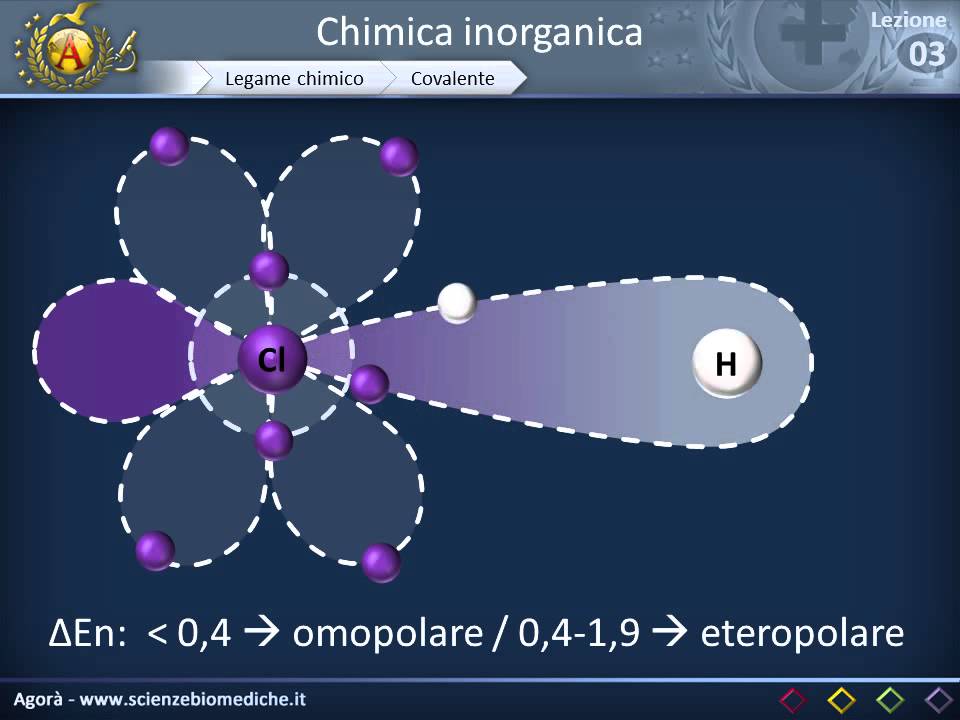
Bentornati nella playlist di chimica oggi dopo aver visto il legame covalente soprattutto quello definibile apolare oppure andiamo a vedere il legame covalente polare prima di iniziare questa lezione Vi ricordo che se vi trovaste bene a studiare con il mio canale e se voleste sostenere il mio lavoro potete fare una donazione tramite il link che trovate in descrizione io come sempre Vi ringrazio anticipatamente Adesso però passiamo a vedere che cos'è il legame covalente polare iniziamo a riprendere la classificazione che abbiamo già visto e cioè il legame covalente può essere definito puro apolare o omopolare se la differenza di elettronegatività tra gli atomi coinvolti nel legame e minore di 0. 4 questo cosa vuol dire vuol dire che se abbiamo due atomi uguali che si legano andranno a formare un legame covalente puro questo però vuole anche dire che se gli atomi che si legano sono diversi il legame covalente potrebbe essere sempre più polarizzato in relazione a quanta E appunto la differenza di elettronegatività tra i due atomi e ricordiamo che l'elettronegatività è quanto un atomo attira gli elettroni ma non solo i suoi anche quelli degli altri Quindi se un atomos attirare maggiormente gli elettroni vuol dire che quel legame che appunto costituito da elettronico condivisi questi elettroni condivisi del legame saranno più attirati da un atomo rispetto che dall'altro è uno dice Beh ma cosa mi interessa a me se gli elettroni vanno più da una parte o dall'altra Beh invece è molto importante perché se gli elettroni avendo una carica negativa si spostano più verso un atomo tutta quella parte della molecola avrà una carica più negativa rispetto all'altro lato della molecola quindi si vanno a formare dei Poli un po' come una pila no che c'è il polo positivo il polo negativo e questo cosa comporta Beh comporta tantissime proprietà che noi vediamo nella vita di tutti i giorni anche solo per quanto riguarda l'ebollizione dell'acqua o il fatto di poter scegliere delle sostanze dentro le altre però in questo momento noi non ci soffermiamo eccessivamente Ma andiamo a capire principalmente Che cos'è un legame covalente appunto dicevamo polare queste elettronegatività dove la troviamo la troviamo su una tavola periodica che però ci deve essere ovviamente scritta perché in tutte le tavole periodiche ci possono essere tantissimi dati tutti questi dati non è detto che ci servono tutti in questo momento Ci serve trovare l'elettrone negatività secondo il metodo di pauling che appunto un chimico che ha stilato questa scala di elettronegatività che è la più utilizzata ve lo proiettata qua Vedete bene come gli elementi a sinistra nella tavola periodica hanno elettronegatività molto bassa i metalli quindi mentre non metalli hanno un elettronegatività relativamente alta l'elettronegatività ricordiamolo cresce da Basso sinistra ad alto a destra Infatti vediamo in alto a destra c'è il fluoro che quello con elettronegatività maggiore di tutti ricordiamo Tra l'altro che il legame covalente soprattutto legame covalente puro e poi anche quello polare avviene solitamente tra atomi di non metalli andremo a vedere poi successivamente cosa succede tra un metallo e non metallo ma ecco vediamo principalmente questi tipi di legami covalenti tra atomi di non metalli quindi tra atomi di elementi che si trovano a destra della tavola periodica e adesso andiamo a vedere come si forma questo legame covalente polare prendiamo ad esempio due elementi l'idrogeno e il cloro l'idrogeno ha un solo elettrone di Valenza Quindi a un solo elettrone nello strato più esterno mentre il cloro ne ha 7 di elettroni di Valenza quindi a 7 elettroni sullo strato più esterno ora la cosa molto importante da sapere è che questi due elementi hanno le tre negatività relativamente abbastanza distanti e cioè l'idrogeno a 2. 2 mentre il cloro ha 3.
16 Ora noi sappiamo che secondo la regola dell'ottetto l'idrogeno vorrebbe avere un elettrone il cloro ne vorrebbe anche lui Uno perché così avendone già 7 se qualcuno gli condivide un elettrone e lui arriva a 8 l'idrogeno avendo 2001 lui vorrebbe arrivare a 2 Ecco l'idrogeno una delle poche eccezioni che ci sono nella tavola periodica che non vogliono raggiungere l'ottetto ma il duetto l'altro atomo è ovviamente l'elio che ha già raggiunto il duetto perché un gas nobile però rimaniamo su quello di cui stavamo parlando ecco l'idrogeno vorrebbe un elettrone il cloro anche vorrebbe un elettrone E allora noi già sappiamo che atomi di natura diversa possono mettere in compartecipazione quindi in condivisione i loro elettroni di Valenza ma esercitano sugli elettroni di legame una differente forza attrattiva questo lo abbiamo appena detto perché appunto c'è una differente elettronegatività in questo caso se l'elettronegatività supera la differenza Scusatemi di elettronegatività super a 0. 4 si forma un legame covalente polare E allora andiamo a vedere Innanzitutto vediamo cosa vuol dire che si forma un legame covalente l'idrogeno e il cloro mettono in condivisione come stavamo dicendo un elettrone a testa questi due elettroni ora sono condivisi cioè fanno parte quindi tutti e due gli atomi vanno a costituire quello che viene chiamato orbitale molecolare e faccio una piccola precisazione io gli elettroni ve li ho disegnati in mezzo ai due atomi però Sarebbe più giusto dire che passano un egual tempo intorno a un atomo e intorno all'altro atomo cioè quegli elettroni ruotano non stanno lì Fermi Ecco questa è una cosa importante da sapere però noi coi disegnini possiamo semplificare tutte Quindi diciamo che con un legame covalente classico quei due elettroni possono stare lì in mezzo vengono condivisi da entrambi gli atomi Ora però come vi ho messo in slide la differenza di elettronegatività è di 0. 96 quindi ampiamente sopra lo 0.
4 Questo vuol dire che il cloro che è la elettronegatività maggiore tenderà Ad attrarre a sé questi elettroni di legame l'idrogeno invece che hanno elettronegatività minore non ce la fa a tenerli ancorati a se stesso e quindi abbiamo che questi elettroni si sposteranno leggermente verso il cloro quanto leggermente Si sposteranno beh si sposteranno in base a quanta differenza di elettronegatività c'è tra i due elementi Cioè se il cloro è tanto più elettronegativo dell'altro elemento attirerà molto più assai elettroni che ci sposteranno molto di più verso di lui ora però bisogna tener presente una cosa che questi elettroni non sono neutri ma l'elettrone una carica una carica negativa e se noi spostiamo la carica negativa da un lato della molecola Ecco che quel lato della molecola diventerà più negativo e di conseguenza l'altro lato diventerà più positivo ed ecco che quindi si andrà a formare un orbitale molecolare sbilanciato in base alle cariche Perché avremo una zona cioè dove c'è l'idrogeno che avrà una parziale carica positiva e lo segnaliamo con questo simbolo che un Delta minuscolo Quindi Delta più mentre dall'altro lato della molecola ci sarà una zona con una parziale carica positiva e lo simboleggiamo con il Delta meno Quindi ripeto quei imbolini del tapio Delta meno vogliono dire parziale vuol dire che il cloro non gli ha rubato l'elettrone non è che se lo tiene tutto per lui l'elettrone continua a girare un po' intorno all'idrogeno ma molto di più intorno al cloro poco intorno all'idrogeno ogni tanto si fa un giro intorno a idrogeno però si fa molti peggiori intorno al cloro Quindi abbiamo che la maggior parte del tempo La zona in cui c'è il cloro sarà caricata negativamente Mentre per la maggior parte del tempo La zona molecolare in cui c'è l'idrogeno avrà una carica parzialmente positiva perché appunto non avrà quell'elettrone che si troverà invece intorno al cloro ricordiamo l'idrogeno a un protone un elettrone se noi gli togliamo l'elettrone Ovviamente rimane il protone quindi la carica più si va a formare quindi una molecola sbilanciata una molecola polare cioè con due poli e appunto la chiamiamo proprio perché ha due poli La chiamiamo dipolo e cioè una molecola con un polo parzialmente positivo e un polo parzialmente negativo gli elettroni quindi non si trovano più al centro fare ai due atomi anzi è più giusto dire che non ruotano egualtempo intorno a tutti e due gli atomi ma sono più spostati o meglio passano più tempo verso l'atomo a Maggiore elettronegatività su cui si forma una parziale carica negativa mentre l'altro atomo di conseguenza acquisirà una parziale carica positiva tanto è maggiore la differenza in determinati attività tra i due atomi tanto più e polarizzato il legame che li unisce e abbiamo detto quindi che questa molecola la chiameremo dipolo Ed ecco che noi abbiamo fatto tutto questo esempio utilizzando L'acido cloridrico Cioè questo composto chiamato hcl o acido cloridrico ma ne esistono tantissimi di composti polari uno tra l'altro ve lo nominato Inizio lezione e andiamone a vedere qualcuno adesso prima di tutto c'è un composto molto simile HF sappiamo che il fluoro è molto simile al cloro perché è sempre una alogeno lo troviamo nel Settimo gruppo della tavola periodica 7 elettroni di Valenza quindi perché se si trova vicino all'idrogeno tenderà a fare un legame covalente questo legame covalente però sarà nettamente polarizzato perché l'idrogeno ha 2. 2 mentre il fluoro abbiamo visto prima quasi quattro di elettronegatività di differenza di elettronegatività Quindi sarà molto molto elevata sarà al limite di 1.