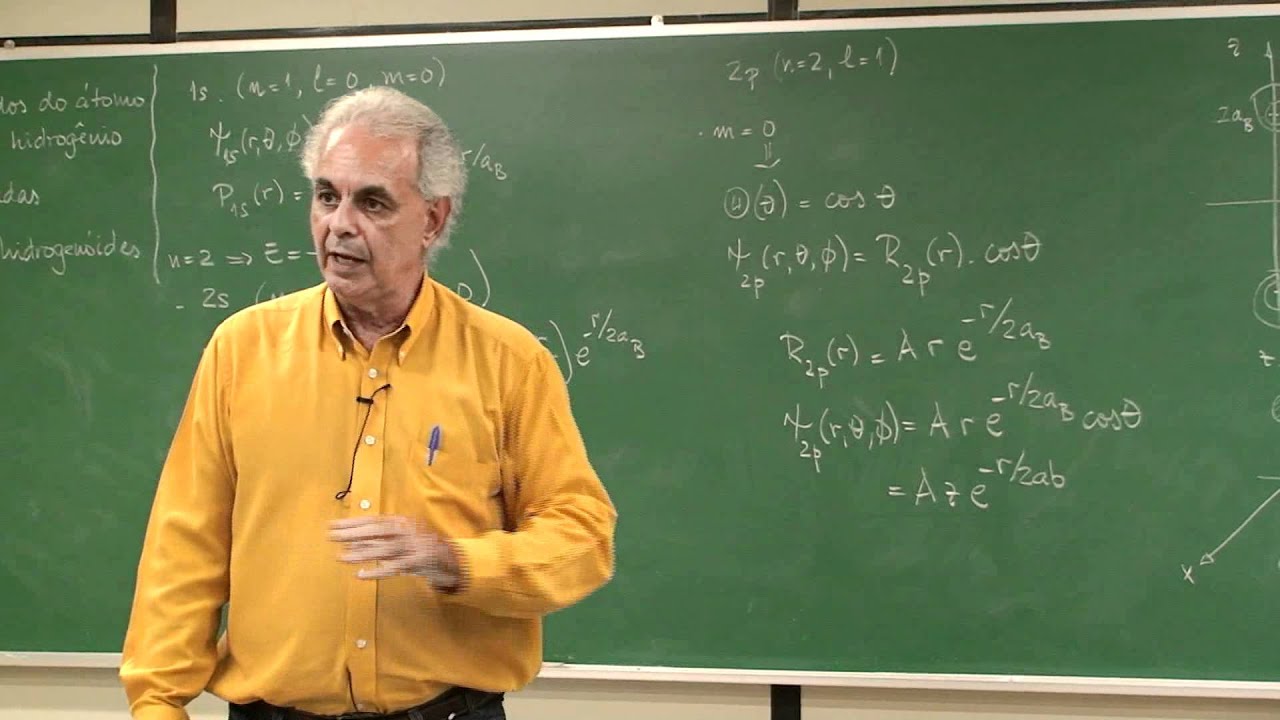na aula de hoje nós vamos estudar as funções de onda obtidas para o átomo de hidrogênio Nós aprendemos na última aula que a resolução da equação de schrodinger nos dá como soluções as funções de onda que descrevem os orbitais atômicos e que cada uma dessas funções é definida pelos números quânticos n l e ML Além disso nós vimos que a densidade de probabilidade eletrônica para o átomo consiste na função de onda PSI elevado ao quadrado se você ainda não viu a aula sobre as funções de onda e os orbitais atômicos o link da mesma estará
na descrição desse vídeo as funções de onda são comumente expressas em coordenadas esféricas sendo PSI uma função de R que a distância em relação ao núcleo mas também Depende de dois ângulos os ângulos teta e f podemos pensar nesses ângulos como latitude e longitude respectivamente nós podemos dividir a função de onda em duas partes uma parte Radial e uma parte angular sendo que a parte Radial nos dá a dependência de PS em função da distância R ao núcleo e a parte angular a dependência de psi em função dos ângulos teta e phi vamos agora analisar
as funções de onda PSI 10000 referente ao orbital 1s e a função PSI 20000 referente ao orbital 2s Como dito anteriormente as duas funções foram divididas em suas partes Radial e angular Observe que a parte angular dessas funções é uma constante ou seja são independentes dos ângulos teta e phi podemos dizer então que a densidade de probabilidade dependerá apenas da distância em relação ao núcleo e os orbitais S são então esfericamente simétricos relação ao núcleo atmico agora vamos observ a parte Radial das funções PS1 e PSI Z consiste na carga nuclear do átomo e a
zer o raio da primeira órbita de B para simplificarmos Essas funções podemos agrupar todas as constantes em uma única constante que denominaremos de k1s para PS1 e k2s para PSI 2 podemos observar que ambas as funções apresentam decaimento exponencial sendo que no caso da função PSI 200 Este decaimento é mais lento temos então que com o aumento do número quântico principal n o raio do Orbital também aumenta já que os orbitais tornam-se mais difusos vamos agora observar graficamente a parte Radial dessas funções no caso da função PSI 20000 podemos notar que há um valor de
R em que a função Radial é igual a zero ao observarmos a equação correspondente a essa função temos que a função é zero quando R = 2 a 0 sobre Z neste ponto há uma inversão de sinal da função de onda o que não ocorre no caso da função correspondente ao orbital 1s bem como o nosso interesse está na probabilidade de se encontrar o elétron devemos elevar ao quadrado as funções radiais e então obteremos os seguintes gráficos Observe que de forma surpreendente existe uma probabilidade finita de encontrarmos o elétron no núcleo do átomo essa característica
de penetração É exclusiva de orbitais s e discutiremos essa questão em aulas posteriores antes de passarmos adiante vamos analisar novamente a função de onda Radial para os orbitais S Como já discutimos anteriormente há um valor de R em que a função Radial correspondente ao orbital 2s é igual a z0 agora observe a função Radial que corresponde ao orbital 3S neste caso há dois valores de R em que a função de onda Radial é igual a zero essas regiões são denominadas de nós radiais se compararmos estes gráficos com os gráficos de densidade de probabilidade veremos que
os nós correspondem a regiões em que a probabilidade de c encontrar o elétron é nula o número de nós radiais para um orbital é dado por N - L - 1 desta forma temos que para a função de onda PSI 10000 que corresponde ao orbital 1s não existe nenhum nó Radial para a função PSI 20000 que corresponde ao orbital 2s há um único nó Radial e para a função PSI 300 que corresponde ao orbital 3S a dois nós radiais e para um orbital 2p quantos nós radiais existem deixa nos comentários se você sabe a resposta
uma outra forma muito interessante de interpretar graficamente as funções de onda consiste em considerar o átomo como sendo composto de várias camadas como se fossem as camadas de uma cebola só que devemos imaginar essas camadas como sendo muito finas com uma espessura DD R Vamos então calcular o volume dessas camadas esféricas nós sabemos que o volume da esfera é dado por 4/3 de PR c e o volume dessa fina camada deve ser então d de v ao derivarmos o volume da esfera em função de R teremos então que D de v é igual a 4
p quadrado DD R ao multiplicarmos a função de densidade Radial ou R qu por ddv teremos então a chamada função de distribuição Radial que nada mais é que a probabilidade de se encontrar o elétron em uma determinada casca esférica em relação ao núcleo aqui temos alguns gráficos de probabilidade Radial ou distribuição Radial para os orbitais 1s 2s e 3S Observe que a probabilidade Radial é igual a z0 em R = 0 isso ocorre pois mesmo que a probabilidade de se encontrar o elétron seja máxima no núcleo o volume da casca esférica é igual a zero
em R = 0 no entanto Como já discutimos anteriormente existe sim densidade eletrônica no núcleo para orbitais s e não devemos considerar essa região como um nó Radial analisando os gráficos de probabilidade Radial para os orbitais 1s 2s e 3S podemos observar também que na medida em que o número quântico n aumenta a região de maior probabilidade de se encontrar o elétron torna-se Mais afastada do núcleo sendo esse um resultado esperado pois nós já sabemos que quanto maior o número n mais difuso é o orbital no caso do Orbital 1s temos que a maior probabilidade
de se encontrar o elétron ocorre quando R igual a a0 ou seja o raio da primeira órbita de bor talvez você se pergunte tudo isso para obtermos o mesmo valor que já obtos utilizando o modelo de bor no entanto temos que ter em mente que aqui estamos tratando de probabilidades o modelo de bor é um modelo determinístico enquanto que o modelo atômico atual é um modelo probabilístico outra forma de se expressar os resultados obtidos consiste em utilizar diagramas de pontos em que os pontos Mais Escuros representam as regiões de maior probabilidade de se encontrar o
elétron e as regiões sem pontos indicam os nós radiais na próxima aula discutiremos alguns dos aspectos mais relevantes dos orbitais p e t para o átomo de hidrogênio Então é isso e até mais [Música]