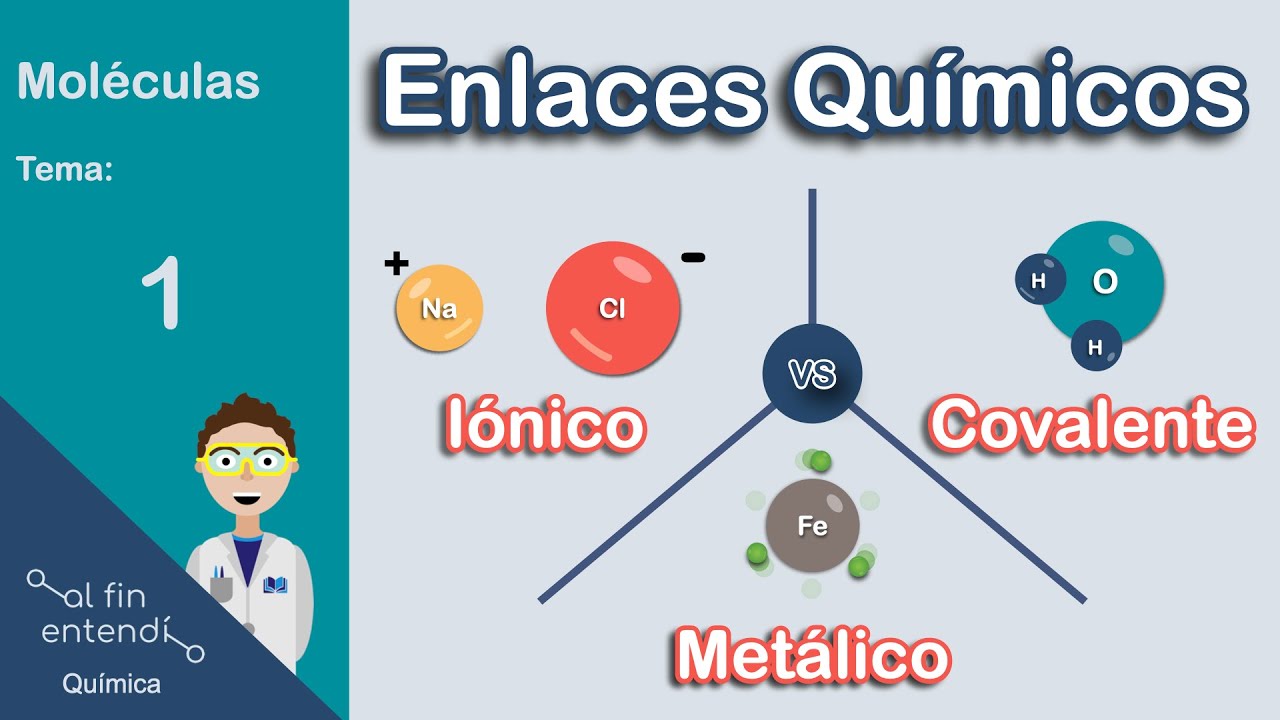
hola a todos en el vídeo anterior dijimos que los enlaces son fuerzas atracción entre átomos para formar moléculas o sea un enlace es cualquier fuerza intra molecular que mantenga los átomos unidos también aprendimos que existen tres tipos básicos de enlaces y que para diferenciar entre un tipo de enlace de otro debemos saber qué elementos participan en él hoy nos enfocaremos en cómo se enlazan los no metales o sea cómo es el enlace covalente este enlace lo vemos mucho cuando se une el carbono y el oxígeno o el hidrógeno al nitrógeno o incluso cuando se unen átomos del mismo elemento por ejemplo cuando formamos una molécula de flúor diatómico aquí vemos los dos átomos de flúor con sus electrones de valencia recuerda que los electrones de valencia son los responsables de formar enlaces por ser los más alejados del núcleo de hecho también mencionamos que los átomos forman enlaces para completar su objeto es decir tener 8 electrones en su estructura de lewis y así ser más estables por ejemplo en el enlace iónico se transferían electrones para que eso ocurriera pero bueno en el caso del enlace covalente de eso no se puede aquí como a cada flor le hace falta solo un electrón para completar su objeto además de que tiene la misma fuerza para traer electrones mejor deciden compartir los electrones eso es un enlace covalente el tener un par de electrones compartidos que unen a dos átomos y literalmente son electrones compartidos o sea que cada flor ya puede decir que completo dos objetos mira que cada átomo tiene tres pares de electrones libres así se les llama los electrones que no participan en el enlace y además tienen un par de electrones en las antes los que si forman el enlace y con eso ya sumarían los 8 electrones totales esa es la principal característica del enlace covalente enlace entre no metales donde se comparten los electrones pero la forma en cómo se comparten estos electrones puede variar y eso va a depender de la electro negatividad de los elementos que estén participando recuerda que la electro negatividad es la capacidad para atraer electrones y aumenta hacia arriba y a la derecha de la tabla periódica por ejemplo observa las diferencias entre un enlace carbono hidrógeno y 1 hidrógeno oxígeno [Música] viste las diferencias vamos con la primera mira los imanes eso representa que la electro negatividad del carbono y del hidrógeno son similares pero la electro negatividad del oxígeno es claramente mucho más grande que la del hidrógeno y es un que afecta aquí ahí te va si vemos los electrones en las antes del carbono y el hidrógeno podemos decir que están hacia la mitad de la distancia entre los dos átomos eso se refiere a que se están compartiendo de manera equitativa ya que ambos elementos tienen casi la misma fuerza para atraer esos electrones muy diferente al enlace oxígeno hidrógeno aquí se ve claro que los electrones están más cerca del oxígeno porque el ala los electrones con mucho más fuerza es más electro negativo o sea que aquí existe una compartición no equitativa o compartición desigual esta es la diferencia entre un enlace covalente no polar y un enlace covalente polar ambos unen átomos no metálicos pero los electrones se comparten de manera distinta eso de compartir electrones es como cuando compartes ropa con un hermano me llegó a pasar que no me alcanzaba para comprar no sé una playera y mi hermano me prestaba para completarla con la condición de que la compartiremos y yo de menso nada pues bueno la compartimos va a estar pareja la cosa pero no compartir ropa con un hermano es como un enlace covalente polar esta playera casi siempre estaba en el closet de mi hermano o peor aún cuando yo la quería usar ella la tarea puesta pero en fin si ahora queremos imaginar al enlace covalente de una forma más realista se utiliza el término densidad electrónica que se refiere a que tanto se concentran los electrones en una región de una molécula por ejemplo si en una molécula hay una región de alta densidad electrónica se refiere a que la mayoría del tiempo los electrones se la viven ahí en cambio en la zona de baja densidad electrónica si hay electrones pero se la pasan muy poco tiempo ahí entonces en el enlace covalente no polar como la compartición es equitativa vemos esto digamos que la densidad electrónica es normal y similar en toda la molécula mientras la compartición desigual del enlace covalente polar produce esto una región con alta densidad electrónica y una de baja densidad es prácticamente lo mismo que el dibujo de arriba solo nos representa que los electrones están más recargados hacia un lado lo que sí importa aquí es que esto produce cargas parciales una carga parcial negativa donde están casi siempre los electrones y una carga parcial positiva donde la densidad electrónica es baja por eso se llama enlace covalente polar porque produce polos uno semi positivo y uno semi negativo después veremos por qué son tan importantes estos dipolos pero hasta aquí creo que ya llevamos mucha información vamos viendo una breve comparación en el enlace iónico se forman cargas netas porque se transfieren electrones de un átomo al otro mientras que en el enlace covalente polar se forman cargas parciales debido a que la densidad de electrón está más cargada hacia un polo de la molécula y en el enlace covalente no polar no hay nada de esto este enlace produce moléculas completamente neutras de hecho para predecir cuál de estos tres casos puede ocurrir cuando se forma un enlace existe una regla que se basa en la electro negatividad de los elementos que participan bueno más específico se basa en la diferencia de electro negatividad que exista entre ellos solo se necesita un cálculo sencillo en el que se resta el valor de electro negatividad del elemento más electro negativo menos el del otro ahorita vemos cómo funciona este cálculo con un ejemplo pero en si esta regla dice que si la diferencia de electro negatividad es mayor a 1. 7 se dará un enlace iónico como el cloruro de sodio que vimos en el vídeo pasado el cloro tiene electro negatividad de 3 y el sodio de 1 por lo tanto la diferencia de electro negatividad sería de 2 en cambio si la diferencia se encuentra entre 1. 7 y 0.
4 resulta en un enlace covalente polar en nuestro ejemplo de del enlace de hidrógeno oxígeno como ocurriría en una molécula la diferencia sería de 0. 9 por eso veíamos las cargas parciales porque el oxígeno si es significativamente más fuerte que el hidrógeno y si la diferencia es menor o igual a 0.